Early eicosapentaenoic acid treatment after percutaneous coronary intervention reduces acute inflammatory responses and ventricular arrhythmias in patients with acute myocardial infarction: a randomized, controlled study.
Int J Cardiol. 2014 Oct 20;176(3):577-82
背景
急性心筋梗塞に対する早期のエイコサペント酸(EPA)のローディングが、CRPを減らすことに伴い、1ヶ月以内の臨床の有害事象を減らすかどうか検証した。急性心筋梗塞は炎症を惹起し、それは心筋障害を引き起こす。EPAは炎症反応を減弱させる可能性がある。
方法
急性心筋梗塞115例をこの前向き、オープンラベル、盲検化、無作為化試験に登録した。EPA群57例と対照群58例に無作為に割り付けた。PCI後24時間以内ににEPA1800mg/日の内服を開始した。主要評価項目は1ヶ月以内の心臓死、脳梗塞、再梗塞、心室性不整脈、発作性心房細動の複合エンドポイントである。
結果
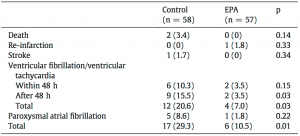
EPAは1ヶ月以内の主要評価項目を著しく減少させ(10.5%vs29.3%, P=0.01)、特に心室性不整脈を減少させた(7.0%vs20.6%, P=0.03)。PCI後のピークCRPはEPA群で低かった(中央値[四分位範囲], 8.2[5.6-10.2]mg/dl vs 9.7[7.6-13.9]mg/dl, P<0.01)。ロジスティック回帰解析では、EPAの使用は1ヶ月以内の心室性不整脈の独立した因子である(オッズ比0.29[95%CI:0.09−0.96])。
結論
急性心筋梗塞に対するPCI後早期のEPA治療は、心室性不整脈とCRP値を減少させる。
◯この論文のPICOはなにか
P:急性心筋梗塞
I:EPA1800mg/日の内服(EPA群)
C:対照群
O:30日以内の心臓死、脳梗塞、再梗塞、心室性不整脈、発作性心房細動の複合エンドポイント
exclusion criteria:心原性ショック、腎不全、心肺停止、緊急CABG、PCIの失敗
手順:PCIの前にアスピリン200mgとクロピドグレル300mgをローディングする。大腿または橈骨動脈アプローチで通常のテクニックでPCIを行う。アクセスを確保した後、ヘパリン10000U投与し、PCI後48時間後まで持続投与する。抗血小板薬はアスピリン100mgとクロピドグレル75mg/日投与する。EPA投与はPCI後24時間以内に開始し、β遮断薬以外の抗不整脈薬の予防的投与は行わない。心室性不整脈や発作性心房細動は、PCI後5日間にわたりホルター心電図をつけ評価する。
定義
心室性不整脈:rate200/min以上で3連以上、またはrate120/min以上で5連以上の心室頻拍、心室細動
◯ランダム化されているか
コンピュータによるランダム化。
◯baselineは同等か
同等。以下、ざっくりと。
年齢70歳、2/3が男性、糖尿病40%、高血圧症70%、喫煙者40%、発症から再灌流までの時間:5時間、責任病変がLAD40%、Killip1/2と3が半々、β遮断薬10%、スタチン10%
◯症例数は十分か
EPAの内服によりprimary endpointの発生が30%から10%に低下すると仮定し、power80%、αlevel0.05として、必要症例数は98例と算出されている。EPA群57例、対照群58例、計115例が登録されている。
◯盲検化されているか
open-labelだが、outcome評価者も盲検化されている。
◯すべての患者の転帰がoutcomeに反映されているか
ランダム化されたすべての患者が解析されている(ITT解析)。
◯感想/批判的吟味
・単施設
・心室性不整脈で主に差がついているわけだが、あくまでサロゲートエンドポイント。
・baselineは同等だが、β遮断薬がどの程度内服していたのか、あるいは血清K値はどの程度の推移だったのかなどはわからない。